上期談到了“蛋白質濃度測定常用的三種方法”,今天繼續就這話題詳解另一種蛋白定量的方法--Bradford 法,至于選用哪種方法,可以根據實驗室的條件和個人喜好來選!做實驗前我們先了解一下實驗原理,如下:
BCA法實驗原理:堿性條件下,蛋白質分子中的肽鍵結構能與Cu2+結合生成紫色絡合物,同時將Cu2+還原為Cu+。BCA試劑可靈敏特異的與Cu+結合,形成穩定的有顏色的絡合物,562nm處有高的吸收值,可在540-595nm測定其吸收值,顏色的深淺與蛋白質濃度成正比,與標準曲線對比,即可計算待測蛋白的濃度。
Bradford 法實驗原理:考馬斯亮藍G250,在游離狀態下呈紅色,大光吸收在488nm;當它與蛋白質結合后變為青色,蛋白質—色素結合物在595nm波長下有大光吸收。其光吸收值與蛋白質含量成正比,因此可用于蛋白質的定量測定。蛋白質與考馬斯亮藍結合在2min左右的時間內達到平衡,完成反應十分迅速;其結合物在室溫下1h內保持穩定。該法試劑配制簡單,操作簡便快捷,反應非常靈敏,靈敏度比Lowry法還高4倍,可測定微克級蛋白質含量。
快速測蛋白法
要想加快速度好是選用 Bradford 法了,這是為什么呢?看Abbkine蛋白質定量試劑盒(Bradford法)優點就知道了:
" 節省時間—顯色反應迅速
" 兼容性好—不受大多數化學物質的影響。對于樣品中巰基乙醇和二硫蘇糖醇的兼容濃度,分別可達1mM和5mM。
" 良好的檢測范圍—檢測范圍為50 - 1000ug/ml。
下圖就是用 Bradford 法測出的標準曲線。雖然線性擬合不佳,但是二項式吻合度卻非常高,可以說非常了。
下圖展示了如何在 excel 中制作二項式標準曲線。
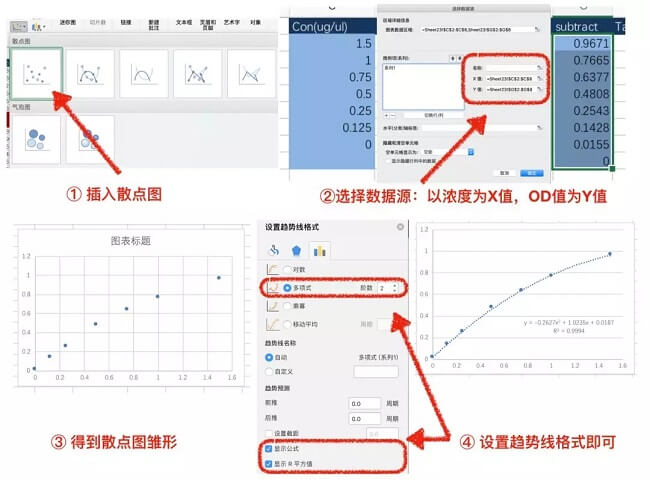
到此為止,前面我們擔心的幾個問題就已經全部解決了。,擔心 Triton 或 SDS 的影響,我們用去垢劑兼容性的 Bradford 試劑即可。第二,擔心標準曲線不佳,我們用二項式來擬合即可。
下面我們繼續利用 excel 的自動化功能進一步提升計算速度。首先,初中的時候大家就學過,解二項式的公式是:
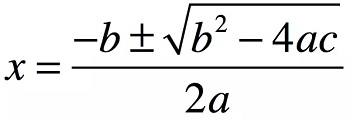
這條曲線是一條開口向下的拋物線,所以取 x 軸上的較小的值就是我們所要的濃度值。為了簡單易用,我們可以先命名幾個單元格為 background,a,b,c,從酶標儀讀取 OD 值之后填入 background,復制標準曲線的光密度值,填入 excel 給出的方程中的 a,b,c 之后,excel 就能自動減去背景計算出濃度了。
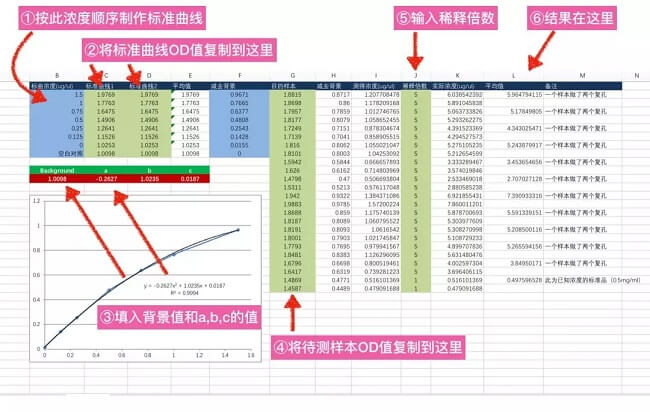
整個過程熟練的話 1 分鐘足矣,操作的同學 2 分鐘也就足夠了。俗話說好馬配好鞍,快速 WB 需得配合快速蛋白定量方能有一氣呵成、唯快不破的痛快淋漓。但是,使用這種方法需要注意的幾個問題:
注意要點
1. 蛋白濃度不能太高,如果超過了標準曲線的范圍(比如 OD>2),那就測量不準了。不僅是本方法,所有基于濃度標準曲線的方法都是如此,比如 ELISA。當然也不能太低了。
2. 大約 10 年前就有文獻報道測量雙波長,即 A595 和 A450 的比值能夠獲得良好的線性關系并提高靈敏度,這種方法我試過了,在 0.125-1.5 mg/ml 的范圍內準確性不如二項式曲線擬合高。
3. 另外,標準品有可能發生降解導致濃度不準確,建議每次測量時加入一個已知濃度的樣本作為校驗。我每次都會加入一個 0.1-0.5 mg/ml 的 BSA 標準品,校驗一下曲線是否準確。
4.加入標準品的時候槍頭一定不能有殘留,否則容易引起較大誤差,建議初學者剛開始時做 2 到 3 個標準品復孔。
5.Bradford 法加完樣之后需立刻馬上測量,OD 值能穩定保持 10 分鐘左右,如果不能馬上測量,建議換用 BCA 法。
6. 大招:如果你已經是老司機了,還有個方法不用測蛋白濃度,只要在顯微鏡下估測各組細胞密度差不多,直接提蛋白變性上樣跑 WB 即可。但老司機也有翻車的時候,請慎用。
請輸入賬號
請輸入密碼
請輸驗證碼
以上信息由企業自行提供,信息內容的真實性、準確性和合法性由相關企業負責,化工儀器網對此不承擔任何保證責任。
溫馨提示:為規避購買風險,建議您在購買產品前務必確認供應商資質及產品質量。