請輸入產品關鍵字:
郵編:200431
聯系人:王小姐
電話:021-56640936
傳真:021-33250231
手機:13122441390 15900755943
留言:發送留言
個性化:www.shifengsj.com
網址:www.shfeng-edu.com
商鋪:http://www.zjmenchuan.com/st236594/
HIV研究亮點進展
點擊次數:874 發布時間:2017-11-16
HIV通過破壞人體的T淋巴細胞,進而阻斷細胞免疫和體液免疫過程,導致免疫系統癱瘓,從而致使各種疾病在人體內蔓延,zui終導致艾滋病。由于HIV的變異極其迅速,難以生產特異性疫苗,至今無有效治療方法,對人類健康造成極大威脅。
據WHO統計,2015年*約有3670萬人HIV攜帶者,其中大部分都在低中等收入國家。據估計2015年新感染HIV的人數約為210萬人。迄今為止已經有3500萬人死于HIV感染,其中2015年有110萬人。
自1987年WHO宣布HIV大流行以來,HIV感染已經導致了3900萬人死亡,目前為止HIV仍然是zui大的公共衛生挑戰之一,因此急需深入研究HIV的功能,以幫助研究人員開發出可以有效對抗這種疾病的新療法。
為阻止病毒大量復制對免疫系統造成損害,HIV感染者需要每天甚至終身服用ART。雖然服用ART已被證明能有效抑制艾滋病發作,但這類藥物價格昂貴、耗時耗力且副作用嚴重。人們急需找到治愈HIV感染的方法。
即將過去的5月份,有哪些重大的HIV研究或發現呢?生物谷小編梳理了一下這個月生物谷報道的HIV研究方面的新聞,供大家閱讀。
1.Mol Ther:重磅!科學家成功利用CRISPR/Cas9消除活體動物的HIV-1感染
doi:10.1016/j.ymthe.2017.03.012
由于病毒能夠在潛在的病毒庫中隱藏起來,因此*治愈HIV感染的愿望目前依然十分渺茫,近日,一項刊登在雜志Molecular Therapy上的研究報告中,來自天普大學和匹茲堡大學的研究人員通過聯合研究發現,他們能夠從活體動物的基因組中切除HIV的DNA從而消除HIV引發的后期感染,同時本文中研究人員也在三種不同的動物模型中實現了這一“壯舉”,包括人源化的小鼠模型(移植入人類免疫細胞的小鼠模型)和感染病毒的小鼠模型等。
文章中,研究者通過研究發現,利用“基因魔剪”CRISPR/Cas9能夠*關閉HIV-1的復制,并且消除動物機體受感染細胞中的病毒。本文研究基于研究人員2016年的一項概念驗證研究,此前研究人員利用轉基因的大鼠和小鼠模型進行研究,研究者將HIV-1的DNA摻入到了動物模型機體每個組織的基因組中;結果發現,這種策略能夠去除實驗動物機體中大部分組織基因組中的HIV-1靶向片段。
研究者Hu表示,這項研究的意義非常重大,我們證實了此前研究的結果,同時也改善了基因編輯策略的效率,同時我們發現這種基因編輯策略在另外兩種小鼠模型中也是有效的,其中一種模型中小鼠細胞表現出急性感染的狀況,另外一種模型在人類細胞中表現出了慢性或潛在的感染。
2.Cell子刊:靶向療法能夠有效清除HIV儲藏庫
doi:10.1016/j.chom.2017.04.011
Gladstone研究所的科學家們zui近發現了一種叫做SMYD2的酶,這種酶可能是一種新的能夠將隱藏的HIV暴露出來的治療靶點。事實上,HIV感染目前仍是zui難以治愈的慢病毒疾病。
雖然藥物療法能夠讓HIV患者過上正常人一樣的生活,但它具有明顯的副作用。此外,患者需要持續性的接受藥物治療才能夠避免隱藏在機體中的病毒重新激活。在感染的早期,HIV隱藏在T細胞儲藏庫中,這種隱藏的病毒會在停止藥物治療之后重新激活。
為了消除HIV儲藏庫,科學家們開發出了"刺激-殺傷"技術,這一技術結合了喚醒病毒功能的藥物并且能夠進一步刺激機體的免疫系統對這些受到感染的細胞進行殺傷。此前的研究在重新激活儲藏庫HIV方面的進展十分有限,因此,科學家們正試圖尋找新的、更加有效的藥物。
"我們的研究重點在一類甲基轉移酶上,這類酶對于HIV的儲藏庫具有重要的調節作用",該文章的*作者,來自Gladstone研究所的研究員Melanie Ott博士說道。"這一種酶對很多疾病的發展同樣具有重要的作用,包括癌癥。也有一些研究試圖尋找靶向的抑制劑進行治療"。
3.HIV 治療的背后:HIV 如何一步步將患者的肺摧毀!
doi:10.1016/j.celrep.2017.04.026
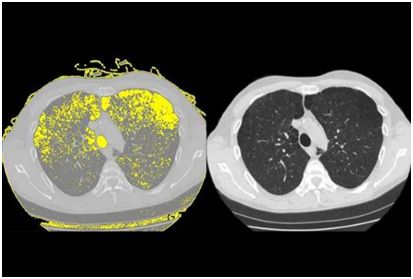
高達 30%的接受抗逆轉錄病毒療法治療的艾滋病毒患者發展為慢性肺病肺氣腫。 Weill Cornell 醫學研究人員的新研究發現了一種可能解釋為什么會發生肺損傷的機制。
研究人員在“細胞報告”5 月 9 日發表的研究報告中顯示,人類免疫缺陷病毒或 HIV 與干細胞結合,稱為基底細胞,其轉化為其他類型的細胞。該過程重新編程基底細胞,導致它們釋放被稱為蛋白酶的酶,其可以破壞肺組織并在進行氧氣交換的空氣囊的壁中戳出孔。
為了進行這項研究,調查人員將正常的人氣道基底細胞從健康非吸煙者的肺部收集,并在觀察下暴露于艾滋病毒一段時間。將病毒與基底細胞表面結合并重新編程,以開始產生可以分解蛋白質并破壞組織的酶或蛋白酶,稱為金屬蛋白酶 -9。因為研究人員知道肺氣腫是氣道疾病,這一發現表明,當基底細胞呈現稱為“破壞性表型”的晶型時,他們開始在健康組織中消失,這會及時得導致肺氣腫。
“看病毒如何改變細胞的功能是一個重要的觀察方面,”Crystal 說,他提到 Zika 病毒通過感染神經干細胞和改變其功能以類似的方式運作,這導致了一個出生缺陷,其特征為小于正常頭部和異常腦,稱為小頭癥。
4.英研究顯示:三藥療法或可延長艾滋病患者壽命
doi:10.1016/S2352-3018(17)30066-8
據法國《20 分鐘報》報道,英國雜志《柳葉刀?艾滋病病毒》(The Lancet HIV) 日前發表了一項研究,稱三藥療法可有效延長艾滋病患者的壽命。男女患者平均壽命分別延長 10 歲和 9 歲,即他們的平均壽命分別可達到 73 歲和 76 歲。
報道稱,自 1996 年引入三藥療法以來,艾滋病患者幾乎已經接近正常人平均 78 歲的壽命。科學家對來自歐洲、北美洲 18 個國家的 88504 名患者數據進行了分析,這些患者在 1996 年至 2010 年間接受了抗逆轉錄病毒治療。結果顯示,2008 年至 2010 年接受治療的患者與 1996 年至 2007 年接受治療的患者相比,前者在治療初期的 3 年中死亡人數更低。
布里斯托爾大學研究員稱,20 年前醫學界已經使用抗逆轉錄病毒療法,但是研發的藥物副作用更小,更好地解決了病毒再生和抗藥性問題。現代治療效果十分明顯,目前他們的問題主要集中于治療的后續過程,艾滋病感染的延遲診斷和多種疾病組合治療以降低感染患者的死亡率。此外,這項研究還指出,隨著時間的推移,治療結果會受到患者行為變化的影響。而壽命的評估建立在死亡率的基礎上,針對年長患者的研究數據不足。
5.抗艾滋病藥物新進展:山東大學藥學院發現新一代抗耐藥性 HIV- 1 抑制劑
doi:10.1021/acs.jmedchem.7b00332
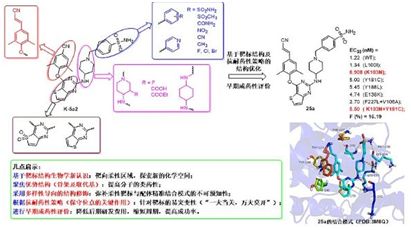
以一代抗艾滋病藥物依曲韋林為先導化合物,山東大學藥學院藥物化學研究所的劉新泳教授課題組與比利時 Leuven 大學醫學院微生物與免疫學研究所合作,發現了一類對 HIV- 1 野生株及多數臨床常見突變株均優于上市藥物依曲韋林的噻吩并嘧啶類化合物,但美中不足的是,代表性化合物 K -2 對臨床zui常見的單突變株 K103N 以及雙突變株 Y181C+K103N 的活性仍有待改善。為進一步提高對這兩種臨床zui常見突變株的活性,該團隊以 K -2 為先導化合物,根據靶標三維空間的適配性要求,特別是蛋白溶劑界面柔性區域的結構特征,綜合運用基于靶標結構的合理藥物設計及抗耐藥性藥物設計策略(形成主鏈氫鍵、靶向保守型氨基酸等),依次對其右翼、中心雜環和左翼進行了系統的結構修飾,以探討未知的化學空間,并完善該類抑制劑的構效關系;采用多樣性導向的結構修飾,可克服柔性靶標與配體結合模式的不可預知性;設計合成了多系列噻吩并嘧啶類 HIV-1 NNRTIs 并進行了細胞及靶點水平的生物活性測試以及早期成藥性評價,zui終發現多個對 HIV- 1 野生株及臨床常見的嚴重耐藥株均有納摩爾水平抑制活性的化合物。
化合物 2(DK5-1)具有抑制 HIV- 1 野生株和多種臨床常見突變株的活性,較先導化合物 K -2 和依曲韋林均有大幅度提高。其中,抑制臨床zui常見的突變株 K103N 的活性(EC50= 0.908 nM)是 K -2 的 3 倍;尤其是抑制臨床嚴重的雙突變株 RES056(EC50 = 5.50 nM)的活性是 K -2 的 6 倍、依曲韋林的 3 倍。對單突變株 L100I、Y181C、Y188L 和 E138K,2 的 EC50 值均小于 5.5 nM,遠優于上市藥物依曲韋林。初步的藥代動力學試驗顯示 2 在大鼠體內達峰時間為 1.7 小時,半衰期為 3.93 小時,并顯示出良好的口服生物利用度(F = 16.19 %)。小鼠急性毒性試驗表明,其 LD50> 2000 mg/kg,心臟毒性試驗結果顯示其抑制 hERG 鉀離子通道的作用較低。目前正在對 2 進行后續的成藥性和臨床前評價。
另外,本文作者還通過分子模擬分析了該類化合物的作用模式及抗耐藥性機理。作者指出,除了 DAPY 類化合物經典的作用力之外,2 的右翼磺酰胺基團可與蛋白溶劑界面的 Lys104 和 Val106 的主鏈之間形成關鍵氫鍵作用,左翼新引入的氰基乙烯基基團指向由高度保守氨基酸 Phe227 和 Trp229 組成的狹長通道,并與之形成緊密的疏水作用,這也是 2 能對多數耐藥株保持抑制活性的主要原因。該研究的一些啟示對其他易突變型或配體結合位點高度柔性靶標的藥物設計具有普遍的參考價值。
6.Sci Rep:重磅發現!感染細胞所釋放的細胞顆粒或能促進HIV感染的擴散
doi:10.1038/s41598-017-01739-8
據美國國家衛生研究院的研究人員的研究顯示,艾滋病毒似乎征服了感染細胞釋放的納米級結構,以感染新細胞。被稱為細胞外囊泡(EVs),這些氣泡狀結構由許多種類的細胞組成,并且在大多數情況下被認為能將分子從一個細胞轉移到另一個細胞,從而提供通信手段。 NIH科學家發現感染艾滋病毒的細胞似乎產生了EVs,其操縱前瞻性宿主細胞將感染傳遞到其他細胞。該研究出現在科學報告中。
在目前的研究中,NICHD的研究人員將HIV和EVs從感染的培養組織中分離出來,將兩者分開,然后測試了在EVs和自己存在下艾滋病病毒感染新培養組織的能力。
由于EVs非常小,難以用常規技術進行分類,研究人員設計了一種新技術來分離和研究它們。研究人員使用了吸引和鎖定特定分子的抗體免疫系統蛋白質。然后,他們將磁性納米粒子化學性連接到抗體上。磁性納米粒子攜帶的抗體在EV或病毒表面上被鎖定到其靶分子上后,研究人員利用磁力將病毒或EV脫離溶液。
當被細胞釋放時,EVs和HIV都攜帶細胞膜中發現的許多蛋白質,Margolis博士解釋說。然而,EV攜帶CD45蛋白和乙酰膽堿酯酶,而HIV則不攜帶。使用針對這些蛋白質的抗體,研究人員能夠將EV從艾滋病毒的實驗室準備工作中剔除。他們發現艾滋病毒感染細胞產生的EVs也在其表面上攜帶有HIV蛋白質,gp120,HIV在感染過程中與細胞結合。
研究人員將EV-缺乏的樣本添加到人類淋巴組織塊時,與保留EVs的對照樣本相比,培養物中的HIV感染率下降了55%。研究人員認為, gp120的損失(如果沒有從艾滋病毒中移除,EVs將能夠提供gp120)會導致艾滋病毒感染的下降。雖然EVs缺乏感染細胞的艾滋病毒RNA,研究人員認為,EV表面上的gp120可以與宿主細胞相互作用,使艾滋病毒更容易感染。
7.Brain Connect:重磅!科學家發現HIV感染或影響機體大腦的連接性及認知表現
doi:10.1089/brain.2016.0457
日前,一項發表于雜志Brain Connectivity上的研究報告中,來自密蘇里大學等研究機構的科學家通過研究發現,相比HIV陰性的年輕人而言,進行有限療法或無任何治療歷史的HIV陽性年輕人的整個大腦結構網絡往往會出現嚴重干擾,而且其大腦神經連接強度和效率也較差,同時這些個體的認知能力也會明顯下降;隨著大腦結構組織異常性的增加,HIV陽性個體的學習能力以及回憶測試的表現也會變得越來越差。
在這項題為“Topological Organization of Whole-Brain White Matter in HIV Infection”的研究報告中,研究者描述了他們的研究發現,即此前沒有進行治療的HIV陽性年輕人的大腦連接往往會出現混亂的狀況;此外研究者還發現,個體的認知表現往往和大腦連接性的改變存在功能性的關聯性。
研究者Laurie Baker表示,這項研究中,我們利用磁共振成像(MRI)對參與者大腦中的白質以及整個大腦網絡結構進行了組織結構的評估,從而確定了在解剖學上的大腦連接性或許能夠作為一種有用且非侵入性的生物標志物來指示HIV感染者大腦中白質的破壞情況。
8.Nat Commun:量子點標記實現活細胞內單拷貝艾滋病毒基因的原位成像
doi:10.1038/ncomms15318
艾滋病毒基因組 RNA 逆轉錄為 DNA,整合在宿主染色體內形成前病毒(HIV provirus),是*艾滋病毒的zui大障礙。在活細胞內對單拷貝或低拷貝的整合態 HIV 基因標記與成像,對前病毒的識別和切除具有重要意義,但一直是個難題。zui近,中國科學院武漢病毒研究所研究員崔宗強與中國科學院生物物理研究所研究員張先恩合作,利用量子點標記轉錄激活子樣效應因子(TALEs)探針,在活細胞內單拷貝基因熒光標記與成像方面取得突破,實現了單拷貝整合態 HIV 前病毒 DNA 原位標記、動態成像和 3D 定位分析。研究成果于 5 月 8 日在《自然 - 通訊》(Nature Communications)在線發表,馬英新和*秀為論文的共同*作者。
研究人員首先設計篩選了特異性識別 HIV- 1 前病毒基因的 TALE 識別元件。基于反式環辛烯(TCO2)與四嗪(Tz1)的生物正交反應,以及鏈霉親和素(SA)與生物素(Biotin)的特異性結合反應,建立活細胞內針對 TALEs 的量子點標記技術。通過“時 - 空耦合”設計,利用不同類型的生物正交反應,獲得不同顏色量子點標記的 TALE 探針。量子點 -TALE 探針特異性標記整合在染色體上的 HIV 前病毒 DNA,實現了活細胞內單拷貝整合態前病毒 DNA 原位標記與成像。在整合 HIV 前病毒 DNA 的潛伏感染細胞中,可以對 HIV 前病毒進行實時動態示蹤和 3D 定位分析,并測定單細胞內整合態前病毒的數目。
該研究實現了活細胞內單拷貝整合態 HIV 基因的熒光標記與成像,對于 HIV 前病毒的高靈敏特異識別和原位分析,以及病毒整合與潛伏感染等關鍵機制的研究和理解均具有重要意義。所建立的量子點 -TALE 探針單基因識別技術,也可以用于其他與疾病和細胞功能相關的任意單拷貝基因的熒光標記與影像分析,為染色體內單基因定位、功能結構和時空動態等研究提供了技術手段。
9.PLoS Pathog:利用新型數學模型解析中和抗體和HIV-1之間相互作用的機制
doi:10.1371/journal.ppat.1006313
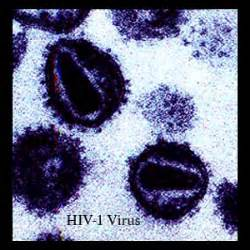
近日,一項刊登在雜志PLoS Pathogens上的研究報告中,來自蘇黎世大學的研究人員通過研究進行實驗和數學分析揭示了HIV-1和抑制病毒在個體間傳播的抗體之間的相互作用,相關研究或為后期科學家們開發治療HIV-1感染的新型療法和疫苗提供了新的希望。
文章中,研究者基于大量證據進行了一項新的分析,研究者表示,能夠靶向作用有害入侵者的特定抗體能夠為機體提供抵御HIV-1的保護作用,盡管研究人員熟知這種抗體所具有的的保護作用,但他們并不清楚抗體和HIV-1之間相互作用的細節。
為了更好地理解二者之間的相互作用,研究人員在文章中對HIV-1和其抗體(中和抗體,nAbs)之間的相互作用進行了深入研究,此前研究中研究者發現,nAbs能夠同嵌入到外膜中的蛋白相互作用,抑制這些蛋白幫助HIV-1躲避宿主細胞的殺滅作用。目前研究者知道,有三種抗體分子能夠結合每一種包膜蛋白,但實驗研究發現,僅有一種抗體能夠有效阻斷病毒包膜蛋白的功能,當結合每個病毒所具有的包膜蛋白數量以及其進入細胞所需要的數量后,研究人員就在實驗室和動物模型機體中進行數學模型模擬出了需要中和HIV-1的nAbs抗體的水平。
利用這種新型模型,研究者就分析了此前在獼猴機體中研究所得的結果,他們認為單一的HIV-1病毒或許會在新宿主中誘發感染,同時研究者還在人類不同性別傳播過程中模擬了nAbs-HIV-1之間的相互作用,并且預測了進行單一性行為時病毒的傳播幾率,以及需要多少nAbs才能夠抑制病毒感染。
10.Nat Commun:病毒和宿主細胞啟動子新認識有望開發出新的HIV治愈策略
doi:10.1038/ncomms15006
動子是基因的一個重要的組成部分,控制著基因表達(轉錄)的起始時間和表達的程度。在一項新的研究中,來自美國伊利諾伊大學厄巴納-香檳分校的研究人員證實病毒和宿主在它們的啟動子上都具有高度類似的調節序列。相關研究結果于2017年5月2日在線發表在Nature Communications期刊上,論文標題為“Similarity in viral and host promoters couples viral reactivation with host cell migration”。
在抗逆轉錄病毒療法停用后,HIV能夠自發性地重新激活。一直以來,不能夠鑒定潛伏的或休眠的HIV感染細胞庫是治愈HIV感染的一個重大障礙。*HIV的主要策略試圖激活這整個潛伏的細胞庫,然后利用當前的藥物混合物清除它。這一方法被稱作“激活并殺死(shock and kill)”療法。
Dar補充道,“在我們的DNA中的基因啟動子和HIV-1病毒啟動子(啟動這種病毒活躍地增殖)在它們的調節上緊密地偶聯在一起,這會導致它們的基因共表達。這是一種潛在的
病毒適應優勢。在這項研究中,我們研究了一種特定的與HIV偶聯在一起的T細胞遷移通路,從而獲得新的治療上的認識。”
11.
移植中的免疫反應或能治愈艾滋病
據《新科學家》雜志3日報道,在上周舉行的歐洲臨床生物學和傳染病會議上,一個研究團隊提交的艾滋病研究數據表明,攜帶艾滋病病毒(HIV)的癌癥患者在接受骨髓移植后,產生的免疫應激反應能夠將病毒*清除。這一研究結果為戰勝艾滋病提供了全新視角。
10年前,一位名叫蒂莫西·布朗的白血病患者在接受骨髓移植治療后,體內的HIV意外地被*清除,他也成為目前世界上*一個被治愈的艾滋病患者。科學界認為,布朗體內HIV*清除應歸功于骨髓捐獻者攜帶的CCR5基因變異,該基因變異能天然抵御HIV,移植后賦予了布朗同樣的能力。
此次,西班牙IrsiCaixa艾滋病研究所和荷蘭烏得勒支大學醫學中心等機構科學家組成的研究團隊公布的數據顯示,另有6位跟布朗一樣身患血癌的HIV攜帶者,在骨髓移植兩年多來體內也檢測不到病毒了。他們下一步會讓這6人停止服用抗艾滋病藥物,以檢測其體內HIV是否*清除。
不過,6人中只有一位的骨髓捐贈者帶有CCR5基因變異。研究人員認為,是移植中普遍存在的抗宿主反應“殺死”了患者的免疫細胞及其體內的HIV,因為這6人在骨髓移植后都患上了移植物抗宿主病(GVHD)。
研究團隊報告稱,共有23位艾滋病患者通過骨髓移植手術來治療血癌,他們中的一半已經因移植物抗宿主病死亡。因此,即便移植后抗宿主反應確實被證明有效,醫生們也不愿故意誘導這種致命性副作用。
12.到2025年結束HIV流行的大計劃!
doi:10.1016/j.amepre.2017.03.012
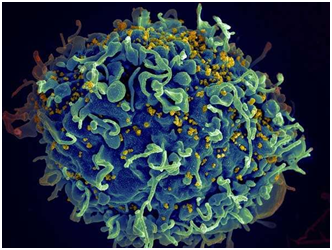
一項新的研究描述了十年前可能似乎無法實現的雄心勃勃但可行的途徑:結束美國艾滋病流行。使用預防監測數據來模擬艾滋病毒發病率,流行率和死亡率,布里格姆和婦女醫院的研究人員制定了目標,特別是到2020年將新感染減少到21,000個人,到2025年將減少到12,000個人,這將標志著結束艾滋病毒/艾滋病流行的過渡。他們的研究結果發表在“美國預防醫學雜志”上。 使用2010年至2013年疾病控制和預防中心的監測數據,該小組模擬了到2025年的許多關鍵指標,包括發病率和流行率,傳播率,死亡率等等。考慮到美國國家艾滋病毒/艾滋病戰略規定的目標(NHAS),如果滿足基準要求,他們將能估計疫情的潛在軌跡。 2020年的國家人權機構目標包括:90%的艾滋病毒感染者知道他們的狀態; 90%的患者將獲得護理; 90%接受抗逆轉錄病毒治療藥物的患者將實現病毒抑制(“90/90/90”目標)。到2020年以后,他們估計將達到2025年要實現的95%的目標(“95/95/95”目標)。
有了這一框架,作者評估了到2025年將新的艾滋病毒感染減少到12,000人是否可以實現。他們使用數學模型發現,到2020年,美國可以實現艾滋病病毒感染發生率降低46%,到2025年艾滋病病毒感染率下降近70%,前提是美國在2020年之前實施了90/90/90艾滋病毒方案框架,95年/ 95/95框架。此外,艾滋病毒傳播率(疫情傳播速度的一個衡量標準)將從2013年的3.53減少到2025年的0.98;艾滋病毒相關死亡人數將從2013年的16,500人降至2025年的12,522人;而美國的艾滋病病毒感染者總人數將從2013年的1 104.6萬人增加到2025年的1,220,615人


 QQ交談
QQ交談